Foto: Reprodução/Freepik
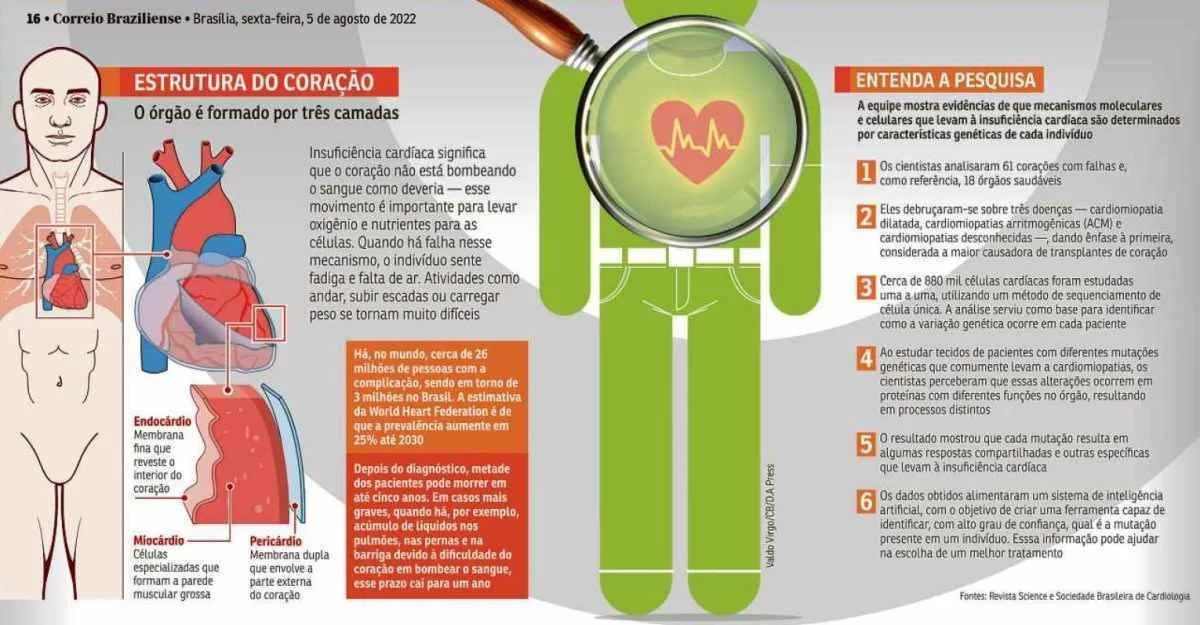
Cientistas de seis países da América do Norte, Europa e Ásia descobriram mutações genéticas que levam pacientes com cardiomiopatia à insuficiência cardíaca (IC). A descoberta, publicada na revista Science, pode resultar em tratamentos específicos com base nos genes de cada pessoa e, na avaliação da equipe, derruba um dogma predominante de que a IC resulta de uma via final comum. "Agora, investigamos mudanças em estágios iniciais da cardiomiopatia que elucidam uma patogênese muito precisa da doença", destaca Eric Lars-Helge Lindberg, pós-doutorando em genética e genômica das doenças cardiovasculares do Max-Delbrück-Centrum für Molekulare Medizin e um dos autores do estudo.
Para realizar a pesquisa, a equipe, composta por 53 cientistas, usou 61 corações com falhas. Como referência, foram utilizados outros 18 órgãos saudáveis. Em torno de 880 mil células cardíacas foram analisadas, uma a uma, através de um método de sequenciamento único. "Até onde sabemos, essa é a primeira análise realizada em tecido cardíaco, e esperamos que essa abordagem possa ser usada para estudar outros tipos de doenças cardíacas genéticas", afirma o coautor sênior, Norbert Hübner.
A partir das análises, os estudiosos identificaram mutações que resultam em processos compartilhados e outros distintos que levam à IC. "Somente esse nível de resolução nos permite ver que as cardiomiopatias não desencadeiam uniformemente as mesmas vias patológicas", enfatiza a coautora sênior, Christine Seidman. A equipe levou em consideração três formas de cardiomiopatia — as desconhecidas, a cardiomiopatia dilatada (CMD) e as cardiomiopatias arritmogênicas (ACM) — e deu foco à CMD, a maior causadora de transplantes de coração e a forma mais comum da doença.
Só no Brasil, cerca de 2 milhões de cardiomiopatias são registradas por ano. No mundo, uma em cada 500 pessoas sofre de alguma variação da doença, somando cerca de 23 milhões de pacientes. O objetivo dos pesquisadores é, diante desse universo de pacientes, desenvolver terapias que possam ser mais individualizadas. Isso significa que cada indivíduo poderia receber um tratamento específico, com base em seu genótipo. Essa forma de tratar pode ser mais eficaz e com menos efeitos colaterais.
Fibrose
A análise mais detalhada também resultou em conhecimentos mais aprofundados sobre algumas complicações cardíacas. "Por exemplo, descobrimos que a fibrose — o crescimento anormal do tecido conjuntivo — observada no CMD não é causada por um aumento do número de fibroblastos no coração", detalha, em nota, Matthias Heinig. "O número dessas células permanece o mesmo. Mas as células existentes se tornam mais ativas e produzem mais matriz extracelular, que preenche o espaço entre as células do tecido conjuntivo", acrescenta Eric Lindberg.
Segundo Henrike Maatz, da Max-Delbrück-Centrum für Molekulare Medizin, na Alemanha, o fenômeno foi especialmente pronunciado nos corações de pacientes com uma proteína específica: o RBM20 mutado. E essa observação também se refletiu nos históricos médicos delas. Geralmente, as que tinham a mutação desenvolveram insuficiência cardíaca e precisaram de um transplante muito mais cedo, comparadas a indivíduos com outras formas genéticas de CMD.
O consórcio disponibilizou todos os resultados obtidos para a comunidade científica. Uma das líderes da pesquisa e professora de medicina na Universidade de Harvard, Christine Seidman espera que esse recurso impulsione estudos de outros grupos para definir novos tratamentos que previnem a IC, que hoje é uma doença incurável. "Esperamos que futuros tratamentos farmacológicos ao menos retardem a progressão da doença, e que os dados de nosso estudo ajudem a fazer isso acontecer", diz o professor do Heart and Diabetes Center NRW Hendrik Milting.
Na avaliação de Milton Henrique Guimarães Júnior, cardiologista da Fundação São Francisco Xavier, em Minas Gerais, a aplicação clínica da descoberta depende de uma cadeia de fatores. "A pesquisa citada pratica a chamada medicina personalizada, com análise de mutações genéticas de cada paciente. Isso necessita de um suporte avançado de laboratórios com testes genéticos, amplamente disponíveis e em larga escala", explica.
Ainda de acordo com o médico, uma possível aplicação não seria fácil considerando a realidade brasileira. O país, diz Guimarães Júnior, ainda luta para oferecer o básico em tratamentos. "Muitos pacientes ainda têm dificuldades para ter acompanhamento regular com cardiologista, acesso aos medicamentos mais novos e a recursos de alta complexidade", afirma.
Caminho para terapias precoces
"A cardiomiopatia define as doenças do músculo do coração (miocárdio) de causas desconhecidas, tais como miocardiopatia idiopática dilatada, miocardiopatia restritiva e miocardiopatia hipertrófica. Os tratamentos são essencialmente clínicos, complementados, em alguns casos, pelas intervenções cirúrgicas, como marcapasso, ressincronizador, cardiodesfibrilador implantável e transplante cardíaco, este com sobrevida média de 10 anos. Essa pesquisa de base celular, 'de bancada', focada em mutações genéticas, poderá abrir caminho para a prevenção e o tratamento precoce, mediante o desenvolvimento de drogas-alvo. A cardiologia brasileira compartilha e participa das principais pesquisas internacionais, incorporando todos os acréscimos do conhecimento da especialidade."
Lázaro Fernandes de Miranda, médico cardiologista do Hospital Santa Lúcia, de Brasília, e conselheiro da Sociedade Brasileira de Cardiologia do DF
Por: Gabriella Tiscoski - Correio Braziliense












0 Comentários
Facebook.com/akiagoraEventos